Por primera vez, investigadores de la Universidad de California en San Francisco han utilizado con éxito el sistema de edición de ADN, CRISPR para alterar los genomas de las bacterias que viven en las entrañas de los mamíferos, un desarrollo que puede avanzar en nuestra comprensión del microbioma y que eventualmente podría allanar el camino para el tratamiento de enfermedades relacionadas con el intestino.
En el estudio, publicado este mes en la revista Cell Reports, los investigadores pudieron eliminar fragmentos de genes de la bacteria Escherichia coli que viven en las entrañas de los ratones y cambiar la composición general de las comunidades bacterianas que pueblan sus sistemas digestivos.
«Hemos demostrado la primera edición de un gen estable dentro del microbioma intestinal de un mamífero. Este es el punto de partida para intentar manipular bacterias en el intestino», dijo Peter Turnbaugh, Ph.D., profesor de Microbiología e Inmunología.
Actualmente, los investigadores y los médicos que desean alterar la microbiota intestinal tienen opciones extremadamente limitadas. La intoxicación alimentaria bacteriana y problemas similares se pueden tratar con antibióticos de amplio espectro, pero estos medicamentos terminan matando muchos microbios «buenos» junto con los malos.
Los trasplantes fecales también se han utilizado con la esperanza de resembrar un microbioma saludable en pacientes con ciertas infecciones y enfermedades gastrointestinales. Pero los médicos no pueden estar seguros de que los microbios introducidos logren superar a las comunidades bacterianas existentes del paciente, lo que significa que el tratamiento no siempre es exitoso.
Por lo tanto, modificar las bacterias que ya prosperan dentro del sistema digestivo será un enfoque clave en la investigación y el tratamiento de problemas de salud relacionados con el microbioma en el futuro, afirmó Turnbaugh. La alteración directa de los genomas de los microbios en el intestino introduciría un nivel de precisión en los tratamientos del microbioma que aún no ha sido posible.
«Ser capaces de alterar el ADN de los microbios que ya se encuentran en el intestino puede permitirnos estudiar el microbioma de una manera más controlada que antes. Realmente nos da la oportunidad de hacer preguntas importantes sobre la salud y la enfermedad», afirmó el investigador.
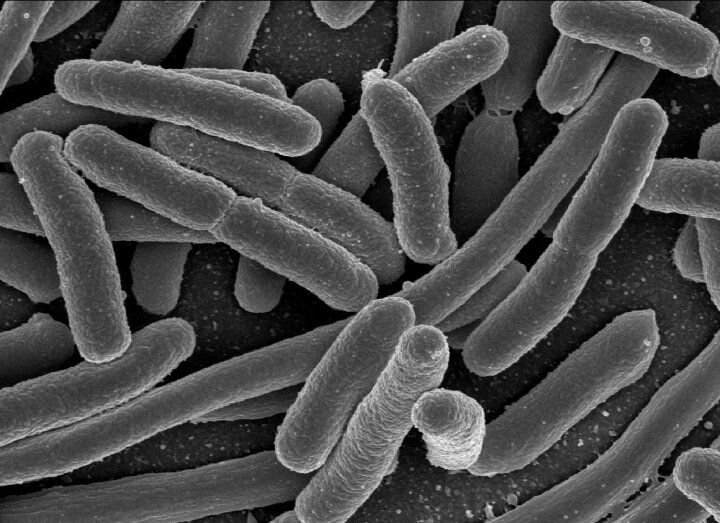
El estudio de Turnbaugh se centró en la E. coli, una bacteria que se encuentra naturalmente en el intestino, pero que tiene mala reputación porque ciertas cepas pueden causar intoxicación alimentaria. Una aplicación útil de la edición de genes de precisión en el microbioma intestinal sería apuntar a cepas dañinas de E. coli sin molestar a las útiles.
Para este estudio, los investigadores querían saber si podían usar la herramienta de edición de genes para atacar y matar una cepa de E. coli dejando otra sola. El equipo de Turnbaugh utilizó un virus, llamado M13, para inyectar un sistema CRISPR-Cas9 en las células de una cepa específica de E. coli, donde se puso a trabajar cortando segmentos de ADN.
Los resultados fueron dramáticos. Antes de que se introdujera el sistema CRISPR-Cas9, la cepa objetivo era más prominente en las muestras fecales recolectadas de los ratones en el experimento. Sin embargo, después de la edición de genes, la cepa objetivo comenzó a desaparecer rápidamente. Después de dos semanas, representó solo el uno por ciento de la población celular monitoreada.
Una clave del éxito del estudio fue el uso de una forma modificada de M13, un virus que ataca naturalmente a E. Coli, pero que normalmente no sobrevive bien dentro del sistema digestivo. Para resolver ese problema, Turnbaugh y sus colegas empalmaron un gen de resistencia a los antibióticos en el ADN que M13 entregaría a las células infectadas, permitiendo que el virus, y el sistema CRISPR-Cas9 que portaba, se propagara más fácilmente.
Turnbaugh prevé que algún día se podría utilizar un enfoque similar para promover el crecimiento de bacterias intestinales «buenas» en los seres humanos. Por ejemplo, si los investigadores editaran genes en ciertas cepas bacterianas para permitir que las bacterias se alimentaran de nutrientes raros, una persona podría obtener cierto control sobre la mezcla de microbios que florecen en su intestino simplemente agregando grandes cantidades de esos nutrientes a su dieta. Primero, dijo, los investigadores deberán expandir la lista de virus en su conjunto de herramientas y experimentar cómo la alteración de miembros individuales del microbioma afecta a la población de bacterias en general.
«El sueño es poder elegir qué cepas específicas de su intestino, o incluso genes individuales, desea promover o eliminar», dijo Turnbaugh. «Estamos realmente entusiasmados con lo lejos que pudimos impulsar esto en E. coli. Esperamos que conduzca a herramientas similares para otros miembros de la microbiota intestinal», concluyó.