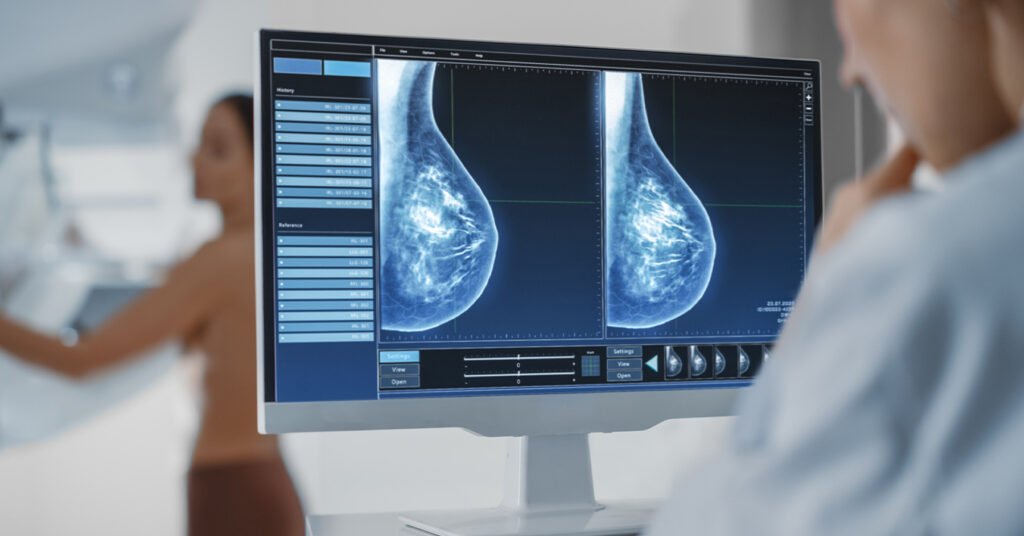
Si bien las mamografías son actualmente el estándar de oro en la detección del cáncer de mama, existen remolinos de controversia: los defensores abogan por la capacidad de salvar vidas (las mujeres de 60 a 69 años tenían un riesgo 33 por ciento menor de morir en comparación con aquellas que no se hicieron las mamografías), y otro campo discute sobre falsos positivos costosos y potencialmente traumáticos (un metanálisis de tres ensayos aleatorios encontró una tasa de sobrediagnóstico del 19 por ciento de la mamografía).
Incluso con algunas vidas salvadas y algunos tratamientos excesivos y pruebas de detección excesivas, las pautas actuales siguen siendo generales: las mujeres de 45 a 54 años deben hacerse mamografías todos los años. Si bien durante mucho tiempo se pensó que la detección personalizada era la respuesta, las herramientas que pueden aprovechar la gran cantidad de datos para hacer esto se quedan atrás.
Esto llevó a los científicos del Laboratorio de Ciencias de la Computación e Inteligencia Artificial (CSAIL) del MIT y de la Clínica Jameel para el Aprendizaje Automático y la Salud a preguntar: ¿Podemos usar el aprendizaje automático para proporcionar una detección personalizada?
De ahí surgió Tempo, una tecnología para crear pautas de detección basadas en el riesgo. Usando un modelo de riesgo basado en IA que analiza quién fue evaluado y cuándo fue diagnosticado, Tempo recomendará que un paciente regrese para una mamografía en un momento específico en el futuro, como seis meses o tres años. La misma política de Tempo se puede adaptar fácilmente a una amplia gama de posibles preferencias de detección, lo que permitiría a los médicos elegir la detección temprana deseada para la compensación de costos de pesquisa.
El modelo se entrenó en un gran conjunto de datos de mamografía de detección del Hospital General de Massachusetts (MGH) y se probó en pacientes retenidos de MGH, así como en conjuntos de datos externos de los hospitales Emory, Karolinska Suecia y Chang Gung Memorial. Usando el algoritmo Mirai de evaluación de riesgos desarrollado previamente por el equipo, Tempo obtuvo una mejor detección temprana que la evaluación anual y requirió un veinticinco por ciento menos de mamografías en general en Karolinska. En MGH, recomendó aproximadamente una mamografía al año y obtuvo un beneficio de detección temprana simulado de aproximadamente cuatro meses y medio mejor.
«Al adaptar la evaluación al riesgo individual del paciente, podemos mejorar los resultados del paciente, reducir el tratamiento excesivo y eliminar las disparidades de salud. Dada la escala masiva de las pruebas de detección del cáncer de mama, con decenas de millones de mujeres que se hacen mamografías cada año, las mejoras en nuestras pautas son inmensamente importantes», señaló Adam Yal, investigador principal.
Medicina profunda
Los primeros usos de la IA en medicina se remontan a la década de 1960, cuando muchos se refieren a los experimentos de Dendral como el punto de partida. Los investigadores crearon un sistema de software que se consideró el primer tipo experto que automatizó la toma de decisiones y el comportamiento de resolución de problemas de los químicos orgánicos. Sesenta años después, la medicina profunda ha evolucionado enormemente en el diagnóstico de medicamentos, la medicina predictiva y la atención al paciente.
«Las pautas actuales dividen a la población en algunos grupos grandes, como menores o mayores de 55 años, y recomiendan la misma frecuencia de detección para todos los miembros de una cohorte. El desarrollo de modelos de riesgo basados ??en IA que operan sobre datos de pacientes sin procesar nos brinda una oportunidad para transformar las pantallas, dando pantallas más frecuentes a quienes las necesitan y ahorrando el resto», apuntó Yala.
Según el investigador, un aspecto clave de estos modelos es que «sus predicciones pueden evolucionar con el tiempo a medida que cambian los datos sin procesar de un paciente, lo que sugiere que las políticas de detección deben estar en sintonía con los cambios en el riesgo y optimizarse durante largos períodos de datos del paciente».
Tempo utiliza el aprendizaje por refuerzo, un método de aprendizaje automático ampliamente conocido por su éxito en juegos como Chess and Go, para desarrollar una «política» que predice una recomendación de seguimiento para cada paciente.
Los datos de entrenamiento aquí solo tenían información sobre el riesgo de un paciente en los momentos en que se tomó su mamografía (cuando tenían 50 o 55 años, por ejemplo). El equipo necesitaba la evaluación del riesgo en puntos intermedios, por lo que diseñó su algoritmo para conocer el riesgo de un paciente en puntos de tiempo no observados a partir de sus exámenes de detección observados, que evolucionaron a medida que se dispuso de nuevas mamografías del paciente.
El equipo primero entrenó una red neuronal para predecir futuras evaluaciones de riesgo dadas las anteriores. Luego, este modelo estima el riesgo del paciente en puntos de tiempo no observados y permite la simulación de las políticas de detección basadas en el riesgo. Luego, entrenaron esa política (también una red neuronal) para maximizar la recompensa (por ejemplo, la combinación de detección temprana y costo de detección) para el conjunto de entrenamiento retrospectivo. Eventualmente, obtendría una recomendación sobre cuándo regresar para la próxima pantalla, que oscila entre seis meses y tres años en el futuro, en múltiplos de seis meses; el estándar es solo uno o dos años.
Digamos que el paciente A viene para su primera mamografía y finalmente recibe el diagnóstico en el cuarto año. En el año dos, no hay nada, por lo que no regresan hasta dentro de dos años, pero luego, en el año cuatro, reciben un diagnóstico. Ahora ha habido dos años de intervalo entre la última pantalla, donde podría haber crecido un tumor.
Usando Tempo, en esa primera mamografía, año cero, la recomendación podría haber sido volver en dos años. Y luego, en el segundo año, podría haber visto que el riesgo es alto y recomendado que el paciente volviera en seis meses y, en el mejor de los casos, sería detectable. El modelo cambia dinámicamente la frecuencia de detección del paciente, en función de cómo cambia el perfil de riesgo.
Tempo utiliza una métrica simple para la detección temprana, que supone que el cáncer se puede detectar hasta con 18 meses de anticipación. Si bien Tempo superó las pautas actuales en diferentes entornos de esta suposición (seis meses, doce meses), ninguna de estas suposiciones es perfecta ya que el potencial de detección temprana de un tumor depende de las características de ese tumor. El equipo sugirió que el trabajo de seguimiento utilizando modelos de crecimiento tumoral podría abordar este problema.
Además, la métrica del costo de detección, que cuenta el volumen total de detección recomendado por Tempo, no brinda un análisis completo de todo el costo futuro porque no cuantifica explícitamente los riesgos de falsos positivos o los daños adicionales de detección.
Hay muchas direcciones futuras que pueden mejorar aún más los algoritmos de detección personalizados. El equipo dijo que una vía sería aprovechar las métricas utilizadas para estimar la detección temprana y los costos de detección a partir de datos retrospectivos, lo que daría como resultado pautas más refinadas. Tempo también podría adaptarse para incluir diferentes tipos de recomendaciones de detección, como aprovechar la resonancia magnética o las mamografías, y el trabajo futuro podría modelar por separado los costos y beneficios de cada uno. Con mejores políticas de detección, podría ser factible volver a calcular la edad más temprana y más tardía en que la detección sigue siendo rentable para un paciente.
«Nuestro marco es flexible y se puede utilizar fácilmente para otras enfermedades, otras formas de modelos de riesgo y otras definiciones de beneficio de detección temprana o costo de detección. Esperamos que la utilidad de Tempo continúe mejorando a medida que se refinan aún más los modelos de riesgo y las métricas de resultados. Estamos entusiasmados de trabajar con socios hospitalarios para estudiar prospectivamente esta tecnología y ayudarnos a mejorar aún más la detección personalizada del cáncer», sostuvo Yala.