Utilizando inteligencia artificial, los científicos del Ludwig Cancer Research desarrollaron un poderoso modelo predictivo para identificar las células inmunes que matan el cáncer más potentes para su uso en inmunoterapias contra el cáncer.
Combinado con algoritmos adicionales, el modelo predictivo se puede aplicar a tratamientos personalizados contra el cáncer que adaptan la terapia a la composición celular única de los tumores de cada paciente.
“La implementación de la inteligencia artificial en la terapia celular es nueva y puede cambiar las reglas del juego, ofreciendo nuevas opciones clínicas a los pacientes”, dijo Alexandre Harari, del Ludwig Lausanne, quien dirigió el estudio con el estudiante graduado Rémy Pétremand.
La inmunoterapia celular implica extraer células inmunes del tumor de un paciente, opcionalmente diseñarlas para mejorar sus capacidades naturales para combatir el cáncer y reintroducirlas en el cuerpo después de que se hayan expandido en cultivo. Las células T son uno de los dos tipos principales de glóbulos blancos, o linfocitos, que circulan en la sangre y patrullan en busca de células cancerosas o infectadas por virus.
Las células T que penetran en los tumores sólidos se conocen como linfocitos infiltrantes de tumores o TIL. Sin embargo, no todos los TIL son eficaces para reconocer y atacar las células tumorales.
“De hecho, sólo una fracción es reactiva al tumor; la mayoría son espectadores. El desafío que nos propusimos fue identificar los pocos TIL que están equipados con receptores de células T capaces de reconocer antígenos en el tumor”, explicó Harari.
Modelo predictivo
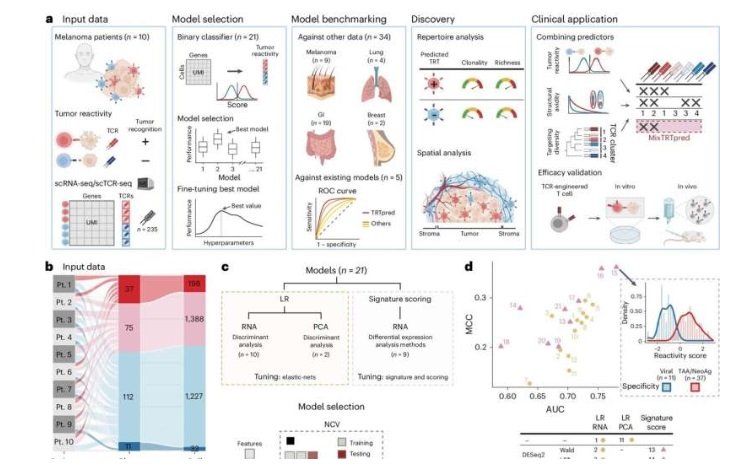
Para ello, el equipo desarrolló un nuevo modelo predictivo impulsado por IA, llamado TRTpred, que puede clasificar los receptores de células T (TCR) en función de su reactividad tumoral. Para desarrollar TRTpred, utilizaron 235 TCR recopilados de pacientes con melanoma metastásico , ya clasificados como reactivos o no reactivos al tumor.
“TRTpred puede aprender de una población de células T y crear una regla que luego puede aplicarse a una nueva población. Así, cuando se enfrenta a un nuevo TCR, el modelo puede leer su perfil transcriptómico y predecir si es reactivo al tumor o no”, agregó Harari.
“TRTpred es exclusivamente un predictor de si un TCR es reactivo al tumor o no. Pero algunos TCR reactivos a los tumores se unen muy fuertemente a las células tumorales y, por lo tanto, son muy eficaces, mientras que otros sólo lo hacen de forma perezosa. Distinguir los aglutinantes fuertes de los débiles se traduce en eficacia”, planteó el investigador.
El estudio demostró que las células T marcadas por TRTpred y el algoritmo secundario como reactivas al tumor y con alta avidez se encontraban con mayor frecuencia incrustadas dentro de los tumores que en el tejido de soporte adyacente, conocido como estroma. Este hallazgo se alinea con otras investigaciones que muestran que las células T efectivas generalmente penetran profundamente en los islotes tumorales.
Luego, el equipo introdujo un tercer filtro para maximizar el reconocimiento de diversos antígenos tumorales. “Lo que queremos es maximizar las posibilidades de que los TIL se dirijan a tantos antígenos diferentes como sea posible”, sostuvo el experto.
Los investigadores llaman a la combinación de TRTpred y los filtros algorítmicos MixTRTpred.
“Este método promete superar algunas de las deficiencias de la terapia actual basada en TIL, especialmente para los pacientes que padecen tumores que no responden a este tipo de terapias en la actualidad”, afirmó el director de Ludwig Lausanne, George Coukos, coautor del estudio que planea lanzar un ensayo clínico de fase I que probará la tecnología en pacientes.
“Nuestros esfuerzos conjuntos darán lugar a un tipo completamente nuevo de terapia con células T”, indicó.